程序性死亡配体1(Programmed Death-Ligand 1,PD-L1)是介导肿瘤免疫逃逸的关键免疫检查点蛋白。它广泛表达于多种肿瘤细胞表面,通过与T细胞表面的程序性死亡受体1(PD-1)结合,向免疫系统发出“don’t find/kill me(别找我/别杀我)”信号,使肿瘤细胞得以逃避免疫清除。PD-L1/PD-1通路的发现推动了癌症免疫治疗的重大突破,相关研究荣获2018年诺贝尔生理学或医学奖。然而,PD-L1在细胞质膜上纳米尺度空间组织分布特性仍未被探索。
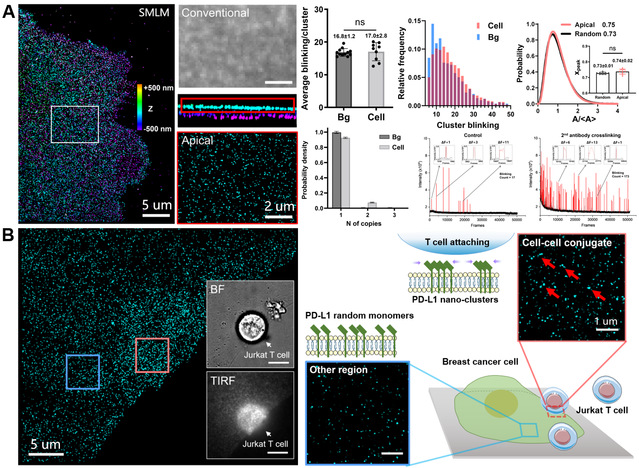
近日,大陆a片 潘雷霆教授、许京军教授团队在PD-L1蛋白超分辨成像研究中取得重要进展。研究团队以人三阴乳腺癌细胞系MDA-MB-231为研究对象,应用单分子定位超分辨成像技术(Single-Molecule Localization Super-Resolution Microscopy, SMLM),并发展闪烁(Blinking)分析、Voronoï分析及Ripley’s K曲线分析等多种定量方法,发现PD-L1主要以单体而非聚簇形式随机分布于癌细胞质膜表面。干扰素γ(IFN-γ)、2-脱氧葡萄糖(2-DG)及辛伐他汀(simvastatin)等药物处理可显著调节PD-L1在质膜上的表达密度,但并不改变其单体化分布特征。为进一步探索PD-L1在细胞质膜上的动力学特性,研究团队发展二抗交联结合单分子定位超分辨成像方法,并辅以荧光漂白后恢复(FRAP)实验,揭示出PD-L1具有较高的侧向流动性和聚簇潜能。此外,实验显示传统的多聚甲醛(PFA)固定方法无法有效固定PD-L1,可导致超分辨成像结果呈现聚簇伪像。把癌细胞与T细胞共培养,在二者形成的“免疫突触”(Immunological Synapse)界面处,SMLM成像观察到PD-L1发生了明显的纳米簇集现象。这一发现提示PD-L1可在免疫应答微环境下发生空间重排,聚簇行为可能是强化“don’t find/kill me(别找我/别杀我)”免疫抑制信号的关键机制。
综上,该工作系统揭示了PD-L1纳米尺度空间分布规律与聚簇特性,为深入理解肿瘤免疫逃逸机制和发展新的免疫治疗策略提供了分子层面成像依据。研究成果以“Super-Resolution Microscopy Reveals Nanoscale Arrangement of PD-L1 Immune Checkpoint”为题发表在国际期刊《Chemical & Biomedical Imaging》上。大陆a片 科学大陆a片 博士后邢福临、杨建宇和胡芬副教授为论文共同第一作者,潘雷霆教授为通讯作者。该工作得到了国家重点研发计划和国家自然科学基金等项目资助。
文章链接://pubs.acs.org/doi/10.1021/cbmi.5c00109
编校:潘雷霆
审核:任梦昕





